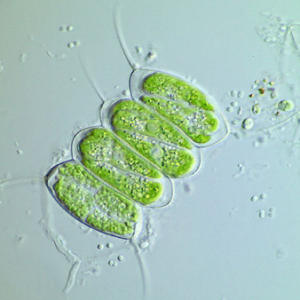
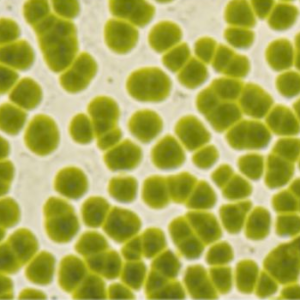
Mat. XIII: Biokraftstoffe auf der Grundlage von Algen- und Bakterien-Stoffwechselprozessen
zurück zur Übersicht
| siehe auch: Haupttext / 3. u. 4. Generation mit allg. Übersicht und weiteren Aufgaben |
Die Herstellung dieser Biokraftstoffe erfolgt unter Verwendung von Mikroalgen, Cyano-, als auch andere -bakterien. Makroalgen kommen nicht zum Einsatz.. Die Organismen-Auswahl und -Optimierung erfolgt weitestgehend nach den Möglichkeiten, die auch in der 3. Generation zum Einsatz kommen (siehe dort: Optimierung ff.). Das heißt, dass die Methoden der modernen Biologie („Protein- oder Metabolic Engineering“, „Synthetische Biologie“) eng mit dieser Generation der Biokraftstoff-Herstellung verbunden sind (siehe AB 15_2.3).
Die Kultivierung erfolgt ausschließlich in Fotobioreaktoren und nicht in offenen Systemen. Dadurch wird zum einen die Gefahr der Infektion der Organismen durch schädliche Bakterien oder Viren reduziert. Zum anderen wird so verhindert, dass genetisch veränderte Organismen freigesetzt werden (siehe Mat. IV). Mögliche Probleme bei der Kultivierung entsprechen denen in der 3. Generation.
Die folgende Abbildung gibt nochmals die wichtigsten Ziele und Grundlagen für die 4. Generation der Biokraftstoff-Herstellung wieder.

Abb. XIII-1 Verwirklichte und angestrebte Ziele der Kraftstoff-Herstellung aus Mikroalgen und Bakterien (vereinfacht)
Im optimierten Stoffwechsel der gewählten Algen- und Bakterienzellen entstehen verschiedene gewünschte „Grundstoffe“. Diese werden in das Medium der Zellumgebung abgegeben und gewissermaßen als „Werkstoff(e)“ durch spezielle Verfahren „abgeschöpft“ und damit dem Bioreaktor entnommen. Die „Zellfabriken“ leben weiter, d.h. sie können im Kreislaufsystem genutzt werden. Auf weiteren möglichst energie- und stoffsparenden Wegen werden diese Werkstoffe dann noch gegebenenfalls zu Neben- und Endprodukten nach den Ansprüchen einer Algen-Raffinerie (siehe Mat. I / (5)) weiterverarbeitet.
| Typen von Fotobioreaktoren für die Kultivierung von Mikroalgen oder Cyanobakterien | ||
Damit keine Missverständnisse aufkommen: Die in den Schemata zur 1. – 3. Generation der Biokraftstoff-Herstellung (z.B. in Mat. XII) enthaltenen „grauen Felder“ weisen auf einen Energie-Input und damit auf CO2-freisetzende Prozesse hin. Selbstverständlich gibt es diesen Energie-Input (Produktionsschritte wie z.B. das Betreiben der Kulturen, Abfall-Entsorgung, Reinigung und Speicherung gewonnener Produkte, etc.) auch in der 4. Generation. Dieser ist hier allerdings aufgrund der Vielfalt der vorhandenen Verfahren und Produktionswege grafisch nicht darstellbar.
Die folgenden Beispiele zeigen exemplarisch Ansätze für mögliche zukünftige Wege in der Biokraftstoff-Herstellung nach Zielen und Grundsätzen der 4. Generation. In den meisten Fällen wird diesbezüglich noch im Labormaßstab oder in Form von Pilotanlagen gearbeitet. Deren Umsetzung und die damit verbundene Anpassung an industrielle Maßstäbe steht noch aus. Das bedeutet natürlich auch, dass diese Verfahren – vorwiegend in Hinblick auf die 1. und 2. Generation der Biokraftstoffe – (noch) nicht wettbewerbsfähig sind.
An vielen Stellen muss noch eine bessere Steuerung von Stoffwechselprozessen, auch in Hinblick auf Faktoren, die störend oder hemmend auf die Stoffproduktion wirken, erreicht werden.
Schließlich muss eine sichere Handhabung der optimierten Mikroorganismen im Rahmen der Biokraftstoff-Herstellung (siehe Mat. XIV) gewährleistet sein.
Biokraftstoffe Bakterien/Algen: Beispiel-1
Elektrolyse als Grundlage für Biokraftstoffe
Dieser Weg der Herstellung von Biokraftstoffen und anderen Produkten beruht auf einer Kombination von Wasserstoff und dem optimierten* mikrobiellem Stoffwechsel bestimmter Cyanobakterien und Grünalgen. Die Gewinnung des Wasserstoffs erfolgt dabei durch Elektrolyse mithilfe von Elektrizität aus erneuerbaren Energien (Solar, Wind und Wasser).
Der gesamte Vorgang wird als mikrobielle Elektrosynthese (MES) bezeichnet. Grundlage ist die Fähigkeit einiger Mikroorganismen, die Elektronen von einer Kathode in den eigenen Stoffwechsel zu übernehmen. Sie werden deshalb auch als elektroaktive Mikroorganismen bezeichnet.
Auf den neuen Stoffwechselwegen werden H2, CO2 und Substrate (evtl. aus speziellen Abwässern und Abgasen) im Rahmen von enzymatischen Prozessen zu neuen Stoffwechselprodukten (Methan, kurzkettige Fettsäuren, Alkoholen, sonstige Chemikalien). Diese werden dann abgeschöpft und gegebenenfalls weiterverarbeitet (= veredelt). Die Zellen selbst bleiben nach der „Sekretion“ der synthetisierten Stoffe im umgebenden Milieu und damit im Kreislaufsystem weiter nutzbar.
Zu den verwendeten Mikroorganismen gehören auch anaerob lebende Bakterien, z.B. verschiedene Clostridien-Stämme. Viele dieser Mikroorganismen sind Krankheitserreger, wie z.B. Clostridium botulinum. Einige besitzen jedoch nutzbare, interessante Stoffwechseleigenschaften. So ist Clostridium ljungdahli in der Lage, Kohlenstoffdioxid in Gegenwart von Wasserstoff zu Ethanol und Essigsäure umzusetzen. Durch genetische Veränderungen wurde bei diesem Bakterium noch weitere Synthesewege geschaffen. Außerdem gelang es, die Fähigkeit CO2 im größeren Umfang zu verwenden maßgeblich zu steigern. Damit konnte nicht nur die Produktmenge erhöht werden, sondern auch ein Beitrag zur CO2-Speicherung geleistet werden.
Weitere Forschungsvorhaben arbeiten nach ähnlichem Prinzip mit Mikroalgen, z.B. der Grünalge Chlamydomonas reinhardtii. Bei ihr wurde die Fotosyntheseleistung optimiert, indem Teile des Stoffwechsels aus dem autotrophen Cyanobakterium Synechococcus sp. in die Grünalge übertragen wurde. Die so von der Alge produzierten Kohlenwasserstoffe konnten sowohl von der Menge, als auch von der Zusammensetzung her beeinflusst werden. Sie wurden u.a. zu Biokraftstoff weiterverarbeitet.
In diesem Arbeitsfeld sind noch viele Probleme zu lösen. So konnte bisher zwar der Übergang von Elektronen auf bestimmte Enzyme nachgewiesen und genutzt werden, die zugrundeliegenden Mechanismen sind nur zum Teil aufgeklärt. Ein weiteres, noch nicht vollständig gelöstes Problem ist der hohe Verschleiß des Elektrodenmaterials.
Die nachweisbare Steigerung der Produktion gewünschter Stoffe, ohne die Mikroorganismen zu zerstören ist jedoch ein wesentlicher Grund, diese Synthesewege weiterzuverfolgen und in größere industrielle Maßstäbe zu übertragen.
Die dabei entstehenden Produkte lassen sich nicht nur als Biokraftstoff nutzen, sondern auch als Quelle für die Synthese „höherwertiger“ organischer Moleküle, die zu verschiedensten Kunst- und Werkstoffen weiterverarbeitet werden können.
*optimiert bedeutet in diesem Zusammenhang: unter Einsatz von biochemischen, gen- und biotechnologischen Verfahren sowie der klassischen Züchtung in Hinblick auf bestimmte Leistungen hin verändert bzw. angepasst. (siehe auch Schema Mat. XII)
Die folgende Linkliste gibt einen kleinen Einblick in dieses relativ junge Arbeitsgebiet der Elektrobiotechnologie (einige in englischer Sprache / letzter Zugriff : 2022-03-10).
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/naturstoffproduktion-mittels-bioelektrosynthese
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/auf-dem-weg-zur-bioelektro-raffinerie
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/trendthema-elektro-biotechnologie
https://de.frontis-energy.com/2019/03/17/fluessigbrennstoff-aus-bio-elektrischen-reaktoren/
https://www.fh-aachen.de/fachbereiche/chemieundbiotechnologie/labore-institute/labor-bioverfahrenstechnik/forschung/elektrochemie-in-bioverfahrenstechnischen-anwendungen
https://www.leibniz-hki.de/de/mikrobielle-bioelektrochemie.html
https://en.wikipedia.org/wiki/Microbial_electrolysis_cell
https://www.uni-bremen.de/uvt/projekte/mikrobielle-elektrosynthese-mit-extremophilen-elektrotrophen-mikroorganismen
https://dechema.de/dechema_media/Downloads/Positionspapiere/2019_Bioelektrosynthese.pdf
https://de.wikipedia.org/wiki/Mikrobielle_Elektrosynthese
https://bioresourcesbioprocessing.springeropen.com/Microbial electrosynthesis of organic chemicals by Clostridium
https://www.derstandard.de/story/2000120347447/mikroorganismen-unter-strom-als-recycling-stars
https://www.sciencedirect.com/science/synthetic biology and microalgal/
https://www.deutschlandfunk.de/bio-solarzellen-mit-cyanobakterien-von-sonnenlicht-zu-100.html
https://bioresourcesbioprocessing.springeropen.com/MES_Clostridium AtCC 25775articles/10.1186/s40643-018-0195-7
Biokraftstoffe Bakterien/Algen: Beispiel-2
Fotosynthese – Schwerpunkt: Lichtabhängige Reaktion (LR)
Wasserstoff wird schon lange auf der Grundlage von fossilen Brennstoffen – Erdgas und Kohle – technisch hergestellt. Weiterhin entsteht Wasserstoff im Rahmen der Biomasseverwertung in der 2. Generation (z.B. Gasifikation, Pyrolyse (siehe Mat. VIII)).
Wasserstoff auf der Grundlage alternativer Energieformen zu erzeugen, setzt auf
- die Nutzung des gewonnenen Stroms aus Windenergie oder Fotovoltaik, verbunden mit der katalytischen Spaltung (= Elektrolyse) von Wasser in Sauerstoff und Wasserstoff, aber auch auf
- optimierte Stoffwechselleistungen von fotosynthetisch aktiven Mikroorganismen zur Wasserstoffgewinnung in Fotobioreaktoren.
Die Möglichkeit, Grünalgen und Cyanobakterien zur Wasserstoffproduktion zu nutzen, wurde realistischer, seitdem die molekulare Aufklärung der Fotosyntheseprozesse weitestgehend abgeschlossen ist. Eine weitere Voraussetzung ist die zunehmende Routine beim Einsatz gen- und biotechnologischer Verfahren. Mit ihrer Hilfe lassen sich die Teilprozesse der Fotosynthese in Hinblick auf die dort arbeitenden Enzyme gezielt verändern.
Von mehreren in diesem Zusammenhang nutzbaren Stoffwechselwegen werden hier zwei – verkürzt und vereinfacht – erläutert.
- Die sogenannte Fotolyse im Rahmen der lichtabhängigen Reaktion der Fotosynthese bezieht sich auf die Absorption von energiereichen Teilchen des Sonnenlichtes durch das Fotosystem II. Dieses System besteht aus einem Enzymkomplex und verschiedenen Pigmenten, z.B. Chlorophyllen.
Im Zusammenwirken aller Beteiligten wird ein Molekül Wasser in zwei Protonen (H+), zwei Elektronen (e–) und ½ O2-Molekül zerlegt (besser lesbar: 2H2O ⇒ 2H2 + 4e– + O2).
Der in den Chloroplasten vorkommende Hydrogenase-Enzym-Komplex (HYDA1) hat die Fähigkeit, die durch die Wasserspaltung freigewordenen Protonen und Elektronen aufzunehmen und wieder abzugeben. Dieses geschieht vorwiegend, wenn viel Lichtenergie „eingefangen“ wird. Auf diese Art und Weise entsteht Wasserstoff (H2), der in die Umgebung abgegeben (Abb. Mat. XIII-7) und „abgeschöpft“ werden kann, ohne den Gesamtprozess der Fotosynthese negativ zu beeinflussen.
Einer der in diesem Zusammenhang am genausten erforschte Organismus ist die Grünalge Chlamydomonas reinhardtii (Abb. Mat. XIII-4 u. 12). Ein noch nicht vollständig gelöstes Problem ist die Sauerstoffproduktion im Rahmen der Fotosynthese, da ein zunehmender O2-Gehalt die Aktivität des genannten Hydrogenase-Komplexes hemmt. Diesbezüglich wird daran gearbeitet, die O2-Toleranz dieser Mikroalge auf der Grundlage genetische Optimierung zu verändern.

Abb. Mat. XIII-7 vereinfachte Darstellung der Fotosynthese im Chloroplasten
(„roter Weg“ = H2-Produktion und Abgabe bei Blockierung des normalen Weges, z.B. mit Hilfe des Hydrogenase-Enzym-Komplexes)
- Bestimmte Cyanobakterien, z.B. Anabaena variabilis (siehe Abb. Mat. AB XIII-10), besitzen Nitrogenasen-Enzym-Komplexe. Ihre Aufgabe besteht darin, molekularen Stickstoff (N2) in biologisch verfügbare Moleküle – NH3 bzw. letztlich NH4+ – umzuwandeln (siehe AB 3_2.3 / Stickstoffkreislauf). Für diese Reaktion werden insgesamt 16 ATP-Moleküle benötigt, um N2 enzymatisch zu NH3 umzuwandeln. Zusätzlich entstehen bei dieser Reaktion zwei Protonen (H+) bzw. ein Wasserstoffmolekül (H2). Bei Stickstoffmangel werden ausschließlich Wasserstoffmoleküle katalysiert und können „abgeschöpft“ werden. Durch gentechnische Maßnahmen konnten diese Prozesse optimiert werden
Weitere Erfolge versprechende Mikroorganismen sind die Grünalge Scenedesmus und weitere Cyanobakterien, z.B. verschiedene Stämme von Arthrospira. Sie sind in der Lage, Wasserstoff aus Sonnenlicht und Wasser zu erzeugen und diesen, sofern er nicht unmittelbar im Stoffwechsel der Mikroorganismen benötigt wird, an die Umgebung abzugeben. Dort kann er ebenfalls „abgeschöpft“ werden.
So einfach die zuvor erläuterten Möglichkeiten der Wasserstoff- bzw. Kraftstoffgewinnung auch klingen, so ist nicht zu übersehen, dass diesbezüglich noch viele Probleme zu lösen sind. Wissenschaftler sehen jedoch in diesen und vergleichbaren Prozessen Möglichkeiten, in Zukunft wettbewerbsfähige Produktionswege im industriellen Maßstab zu entwickeln. Sie sehen darin eine Ergänzung der Wasserstoffgewinnung auf der Grundlage von durch Windenergie gewonnenen Strom.
Die folgende Linkliste gibt einen kleinen Überblick über die Ansätze, Wasserstoff auch mithilfe von Mikroorganismen und nicht nur über den Einsatz von regenerativem Strom zu gewinnen (einige in englischer Sprache / letzter Zugriff : 2022-03-10).
https://de.wikipedia.org/wiki/Biowasserstoff
https://de.wikipedia.org/wiki/Wasserstoffbioreaktor
https://en.wikipedia.org/wiki/Biohydrogen
https://www.golem.de/news/energiewende-mikroreaktoren-aus-algen-erzeugen-wasserstoff-2011-152406.html
https://www.deutschlandfunk.de/bio-solarzellen-mit-cyanobakterien-von-sonnenlicht-zu-100.html
https://futurium.de/de/blog/wasserstoff-aus-der-algenfabrik
https://biooekonomie.de/themen/dossiers/biowasserstoff-quellen-und-forschungsansaetze
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/so-erzeugt-die-natur-wasserstoff-produzierende-enzyme
https://www.energiezukunft.eu/umweltschutz/neuer-ansatz-bei-der-herstellung-von-wasserstoff-aus-algen/
https://www.energieleben.at/wasserstoff-aus-algen/
https://www.energy.gov/eere/fuelcells/hydrogen-production-photobiological
Biokraftstoffe Bakterien/Algen: Beispiel-3
Fotosynthese – Schwerpunkt: Lichtunabhängige Reaktion (LuR)
In der lichtunabhängigen Reaktion (= Calvin-Zyklus) erfolgt die Produktion organischer Kohlenstoffmoleküle. Entsprechend optimierte Mikroorganismen besitzen eine verbesserte Aufnahme von CO2 und produzieren mehr Wasserstoff, als der eigene Organismus benötigt. Dieses führt in der LuR auch zu einer vermehrten Produktion von organischen Kohlenstoffmolekülen. Diese von den Zellen nach außen abgegebenen und „abschöpfbaren“ Stoffwechselprodukte sind z.B. Bioethanol und andere kohlenstoffhaltige organische Stoffe.
Zu den verwendeten Mikroorganismen, gehören Cyanobakterien-Stämme von Anabaena sowie verschiedene Grünalgen, wie z.B. Chlamydomonas und Botryococcus.
| Eine Besonderheit zeigt das u.a. in diesen Zusammenhängen verwendete Cyanobakterium Synechocystis sp. PCC6803. Dieses auch autotroph lebende Süßwasser-Bakterium wird häufig als Modellorganismus verwendet, wenn es gilt, neue Produktionswege zu finden. Es ist das mit am genauesten untersuchte Cyanobakterium, das sich dementsprechend auch am besten gen- und biotechnisch „bearbeiten“ lässt.
Gene aus anderen Mikroorganismen, z.B. aus Zymomonas mobilis (, Bakterium, siehe auch Mat. III) werden verwendet, um bestimmte Stoffwechselwege in diesem Cyanobakterium zu optimieren. Die „Eingriffe“ führen sowohl zur besseren CO2-Aufnahme als auch der Optimierung von Toleranzen gegenüber verschiedensten Umweltfaktoren. Unter anderem wird so Bioethanol in Fotobioreaktoren auf der Grundlage der Umwandlung von Sonnenenergie synthetisiert. Die Gewinnung des von den Zellen abgegebenen Ethanols erfolgt über spezielle Verdampfungstechnologien, wobei der Alkohol in den oberen Raum des Reaktors aufsteigt, an der Innenfläche kondensiert und in Auffangwannen gesammelt wird. Die Cyanobakterien können „ungestört“ weiterarbeiten. |
Und wie sieht es mit der Herstellung von Biodiesel in der 4. Generation aus?
Die Möglichkeit, Algen so zu „gestalten“, dass sie die entsprechenden Öle in der Biomasse speichern, wie z.B. Botryococcus braunii (siehe Abb. Mat. XIII-13) gibt es. Dass sie diese nach außen abgeben, ist das Ziel mehrerer Forschungsansätze. Bisher ist lediglich die Optimierung von Produktionswegen in der Zelle und eine damit verbundene Öl-Speicherung gelungen. Als Verwertungswege stehen bisher nur die Verfahren der 3. Generation zur Verfügung. Das bedeutet jedoch die „Zerstörung“ der Biomasse für die anschließende Ölextraktion oder Gasifikation (siehe Mat. XII).
Die folgende Linkliste führt zu einigen Ansätzen, mithilfe von Mikroorganismen u.a. durch die Optimierung des Calvin-Zyklus, Biokraft- und andere Stoffe zu gewinnen. Einige Quellen sind in englischer Sprache / letzter Zugriff : 2022-03-10).
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/alkohole-direkt-aus-co2-herstellen
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/mikroben-verwandeln-co2-spezialchemie
https://www.biooekonomie-bw.de/fachbeitrag/aktuell/multitalente-cyanobakterien-vom-biosprit-zum-klimaretter
https://www.sciencedirect.com/science/botryococcus_productivity_carbohydrate
https://www.frontiersin.org/articles/transformation_Synechocystis_pcc6803
https://www.frontiersin.org/articles/cyanobacteria_biofuel_production
https://www.mdpi.com/cyanobacteria_potentials
https://www.sciencedirect.com/science/anabaena_algal_refinery
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/mikroben-verwandeln-co2-spezialchemie
https://www.researchgate.net/publication/339421688_Cyanobacteria_as_a_biofuel_source_advances_and_applications
https://de.wikipedia.org/wiki/Synechocystis
https://biotechnologyforbiofuels.biomedcentral.com/articles/10.1186/s13068-020-1660-z
https://link.springer.com/article/chlamydomonas_bioethanol
https://engineering.vanderbilt.edu/news/2021/1-5m-doe-grant-targets-engineering-of-cyanobacteria-as-biofuel-production-platform/
https://www.systembiologie.de/de/aktuelles/wissenschaft/biosprit
Biokraftstoffe Bakterien/Algen: Beispiel-4
Einsatz von Mikroorganismen zur Methangewinnung
Die Methangewinnung ist bereits in einem anderen Zusammenhang thematisiert worden (siehe Mat. IX). Dort geht es allerdings um die Reinigung von herkömmlichem Biogas durch Schwefelbakterien, um möglichst reines Bio-Erdgas (= Methan) zu gewinnen.
In diesem Abschnitt geht es um Methan, das unabhängig von Biogasanlagen gebildet wird. Im Mittelpunkt stehen die Bemühungen, optimierte Mikroorganismen in ihrem Stoffwechsel gezielt Methan produzieren zu lassen und dieses dann „abzuschöpfen“. In einem Exkurs wird aus der Sicht von Wissenschaftlern erläutert, inwiefern Methan in größeren Seen als Bio-Energie-Quelle eine bedeutende Rolle spielen könnte.
Wenn von Power-to-Gas (= PtG) die Rede ist, wird fast immer die Umwandlung von elektrischer regenerativer Energie in Wasserstoff (H2) – Power-to-Hydrogen – gemeint. Grundsätzlich ist diese Vorgehensweise auch anwendbar, um Methan zu erzeugen.
Ein weiterer Weg besteht im Einsatz von optimierten Mikroorganismen, die externes Kohlenstoffdioxid in ihrem Stoffwechsel in Methan umwandeln – Power-to-Methan -, das „abgeschöpft“ werden kann (= biologische o. mikrobielle Methanisierung). Dieser Prozess lässt sich vereinfacht durch folgende Reaktionsgleichung beschreiben: 4 H2 + CO2 ⇒ CH4 + 2H2O
Ein dazu eingesetzter und sehr gut erforschter Organismus ist das Purpurbakterium Rhodopseudomonas palustris. Es handelt sich dabei um ein stäbchenförmiges Bakterium mit am Ende liegenden kurzen Geißeln. Bei Licht zeigt es eine violette Färbung.
Das Bakterium ist fakultativ anaerob (= lebt mit oder ohne Sauerstoff). Auf der Grundlage eines speziellen Enzymkomplexes, einer sogenannten Nitrogenase, ist es in der Lage, Luft-Stickstoff (N2) zu binden. Im Rahmen des Stoffwechsels wird dieser zur Wasserstoffproduktion (H2) und damit zur eigenen Energiegewinnung genutzt. Letztlich entsteht Ammonium (NH4+), das damit für den Stickstoffkreislauf (siehe AB3_2.3) verfügbar gemacht wird.
| Wissenschaftler fanden nun heraus, dass nach Änderung von nur zwei Aminosäuren in diesem Enzymkomplex eine entscheidende Änderung im Stoffwechsel zu beobachten ist. Das Bakterium verliert bei Lichteinfluss die Fähigkeit der Stickstofffixierung, wandelt aber stattdessen Kohlenstoffdioxid (CO2) zu Methan (CH4) um. Die Wasserstoffproduktion erfolgt weiterhin. Die produzierten Gase werden in das umgebende Medium abgegeben, wo es „abgeschöpft“ werden kann. Die momentane Forschung und Verfahrensentwicklung bestehen u.a. darin, die zugrundeliegenden Prozesse genauer zu steuern, d.h. die Ausrichtung auf eines der Produkte gezielt zu fördern oder zu hemmen. Auch bei anderen Mikroorganismen, hauptsächlich Cyanobakterien, werden ähnliche Wege zur Gewinnung von Methan gesucht. Sie sind in eutrophierten* Gewässern die Organismengruppe, die mit zur Methanbildung und -freisetzung führt.Im Rahmen der Forschung bzw. gezielten Nutzung dieser Bakterien zur Methangewinnung muss auch die Freisetzung dieses Gases in die Atmosphäre verhindert werden. Für die Kultivierung und damit auch die CO2-Versorgung entsprechender Mikroorganismen sollen zukünftig vermehrt geeignete Abwässer, Abgase und Schlämme eingesetzt werden. Ausgereifte, d.h. großtechnisch anwendbare Verfahren stehen noch nicht zur Verfügung. Vor allem unter dem Gesichtspunkt des Energieeinsatzes muss diese Art der biologischen Methanisierung noch weiterentwickelt werden.*Eutrophierung: Die natürliche oder durch den Menschen verursachte Anreicherung von Nährsalzen in einem Gewässer führt zu einer explosionsartigen Vermehrung von Algen mit negativen Folgen für das Ökosystem, u.a. sauerstofffreie Zonen. |
| Exkurs: Das Treibhausgas Methan – auch als Energieversorger?
Methan ist ein ca. 23mal wirksameres Treibhausgas als Kohlenstoffdioxid (siehe auch hier). Zu seiner Freisetzung in die Atmosphäre tragen hauptsächlich folgende Ursachen bei: Wiederkäuer, auftauender Permafrostboden, Reisfelder, Mülldeponien, Undichtigkeiten bei der Biogasproduktion, Gewinnung von fossilem Erdgas und Abbau toter organischer Substanz am Gewässerboden. In einem Gewässer wird absinkende tote organische Substanz von aeroben Bakterien abgebaut, solange ausreichend Sauerstoff vorhanden ist. Letztlich werden vor allem Nährsalze und Kohlenstoffdioxid freigesetzt. Wissenschaftler haben sich nun genauer mit den Möglichkeiten beschäftigt, das in größeren und tieferen Gewässern am Grund anfallende Methan für die Energieversorgung zu nutzen. Sie sehen darin zumindest einen weiteren Baustein für die zukünftige Energieversorgung. |
||
Wissenschaftler des Kirchhoff Instituts für Physik und der Umweltphysik an der Universität Heidelberg sowie das Kompetenzzentrum für Nachhaltige Entwicklung an der Universität Tübingen beschäftigen sich mit der folgenden Möglichkeit der Energiegewinnung durch Methan.
Die Wissenschaftler aus Basel weisen darauf hin, dass alle größeren und tieferen Seen auf gleiche Art und Weise Methan speichern, auch in Europa. Es wird geschätzt, dass – theoretisch betrachtet – die weltweit in entsprechenden Seen gespeicherte Methanmengen ausreichen, um den globalen Energiebedarf zu decken. |
|
|
Quellen / Methan aus Seen (Zugriff für alle : 2021-09-01) :
https://www.deutschlandfunkkultur.de/methan-strom-aus-ruanda-energie-aus-dem-vulkansee.979.de.html?dram:article_id=499936
https://www.unibas.ch/de/Aktuell/News/Uni-Research/Kohlenstoff-neutrale-Biotreibstoffe-aus-dem-See.html
https://www.dialog-energie.de/2019/09/10/energieerzeugung-am-kivu-see/
https://www.sueddeutsche.de/wissen/kivu-see-zeitbombe-unter-wasser
https://de.wikipedia.org/wiki/Kiwusee_Die_Sättigung mit Gasen
Die folgende Linkliste gibt einen Einblick in die Ansätze, mithilfe von Mikroorganismen Methan zu gewinnen (einige in englischer Sprache / letzter Zugriff : 2022-03-10).
https://en.wikipedia.org/wiki/Rhodopseudomonas_palustris
https://de.wikipedia.org/wiki/Biologische_Methanisierung
https://de.wikipedia.org/wiki/Methanbildner
https://en.wikipedia.org/wiki/Methanobacteria
https://www.pnas.org/doi/10.1073/pnas.1611043113
https://www.uni-heidelberg.de/de/newsroom/cyanobakterien-produzieren-methan
https://www.nature.com/articles/s41467-019-10996-2#Sec5
https://www.wissenschaft.de/erde-umwelt/auch-cyanobakterien-produzieren-methan/
Biokraftstoffe Bakterien/Algen: Beispiel-5
Einsatz von Mikroorganismen zur Stromgewinnung
Strom bzw. elektrische Energie ist letztlich ebenfalls zu den „Kraftstoffen“ zu zählen.
Elektrischer Strom
Der elektrische Strom (elektrische Energie) ist die gezielte und gerichtete Bewegung freier Ladungsträger. Die Ladungsträger können Elektronen oder Ionen sein. Elektrischer Strom kann nur fließen, wenn zwischen zwei unterschiedlichen elektrischen Ladungen genügend freie und bewegliche Ladungsträger vorhanden sind, z.B. in einem leitfähigen Material (Metall, Flüssigkeit).
gut verständliche Info: https://studyflix.de/elektrotechnik/elektrischer-strom-3237 (Zugang: 2022-03-11)
| Von mikrobiellen Brennstoffzellen (microbial fuel cell (MFC)) spricht man, wenn mithilfe von Mikroorganismen – in der Regel Bakterien – Strom erzeugt wird. Dabei wird die in organischen Stoffen enthaltene chemische Energie von den Bakterien zum Teil in elektrische Energie umgewandelt.
Ausgangspunkt ist die Zellatmung anaerober Bakterien, bei der energiereiche organische Stoffe zur Gewinnung von ATP, Kohlenstoffdioxid und Protonen genutzt werden. Bei diesem Prozess werden durch Oxidation und Reduktion Elektronen (e–) bewegt. Normalerweise werden die Elektronen sofort wiederverwendet. Außerdem entstehen Wasserstoffionen (H+). Anwendung findet dieses Prinzip durch die Behandlung von Abwässern, Schlämmen und feuchten Abfällen. Der Einsatz der elektrochemischen Bakterien kann in diesen Bereich nicht nur die notwendige elektrische Energie für das Betreiben einer Anlage liefern, sondern verringert auch die im Abwasser enthaltenen organischen Stoffe (Abb. Mat. XIII-20). Zu den elektrochemisch aktiven Mikroorganismen gehört auch das bereits in Zusammenhang mit der Methangewinnung genannte Bakterien Rhodopseudomonas palustris. Auf dieser Grundlage wurde ein weiterer Anwendungsbereich entwickelt: Üblicherweise wird der Gehalt an abbaubaren organischen Stoffen in einem Gewässer über eine zeitintensive chemische Messmethode* bestimmt. Durch den Einsatz der elektrochemischen Bakterien lässt sich dagegen eine Echtzeit-Bestimmung dieser Stoffe durchführen: Je mehr abbaubare organische Stoffe vorhanden sind, desto größer ist der Stromfluss und umgekehrt. Ganz am Anfang stehen Forschung und Entwicklung zur Nutzung elektrochemischer Bakterien in Hinblick auf ihren Einsatz als Speichermedien und als Steuerungselemente in Prozessor-Chips. *BSB5: http://www.wasser-wissen.de/abwasserlexikon/b/bsb.htm (Zugriff: 2021-11-02) |
|
|
| Für den naturwissenschaftlichen Unterricht in den USA gibt es einfache Arbeitsanleitungen (Kits), um die Leistungen elektrochemischer Mikroorganismen zu veranschaulichen (siehe Abb. Mat. XIII-21 und Link) (https://www.instructables.com/id/How-to-Make-a-Microbial-Fuel-Cell-MFC-Using-Mud/(Zugriff: 2021-11-02)Hinweis: Die Anleitungen in Kits aus den USA entsprechend nicht immer den deutschen Sicherheitsansprüchen an den naturwissenschaftlichen Unterricht! |
Die folgenden Links geben Einblicke in Arbeiten. Z.T. mit anschaulichen Beispielen, wie mithilfe von Mikroorganismen Strom zu gewinnen und zu nutzen ist (einige in englischer Sprache / letzter Zugriff für alle : 2022-03-10).
https://biooekonomie.de/foerderung/foerderbeispiele/stromerzeugung-mit-mikroben
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/die-mikrobielle-stromproduktion-angekurbelt
https://biooekonomie.de/akteure/interviews/strom-aus-abwasser
https://de.wikipedia.org/wiki/Mikrobielle_Brennstoffzelle
https://letstalkscience.ca/educational-resources/stem-in-context/microbial-fuel-cells
https://www.sciencedirect.com/topics/biochemistry-genetics-and-molecular-biology/microbial-fuel-cell
https://www.hevs.ch/media/document/3/mikrobielle-brennstoffzelle.pdf
http://www.chemgapedia.de/vsengine/biobrennstoffzellen_aufbau_.html
https://de.frontis-energy.com/2021/01/09/mikrobielle-brennstoffzelle-im-pilotmassstab-produziert-strom-aus-abwasser/
https://wiki.edu.vn/wiki21/2021/01/05/shewanella-wikipedia/
Videos zur mikrobiologischen Brennstoffzelle
https://www.youtube.com/Strom aus Klaeranlage
https://www.youtube.com/aus urin strom herstellen
Folgende Links führen zu weiteren Informationen bzw. waren wesentliche Grundlagen für die zuvor erfolgten sehr speziellen Ausführungen. (für alle gilt: letzter Zugriff: 2022-12-13)
Bei Interesse sind viele Artikel zu diesem Thema auffindbar. Allerdings sollte man auch Begriffe in englischer Sprache verwenden, z.B. die Kombination „biofuels 4. generation“.
https://biooekonomie.de/nachrichten/mikroben-verwandeln-co2-spezialchemie
https://biooekonomie.de/video/wenn-aus-abgas-rohstoff-wird
https://biooekonomie.de/nachrichten/alkohole-direkt-aus-co2-herstellen
https://bioresourcesbioprocessing.springeropen.com/articles/Microbial electrosynthesis1 Clostridium
https://pubs.rsc.org/en/content/articlelanding/2018/hydrogen_chlamydomonas
https://www.sciencedaily.com/releases/2018/photosynthetic_biofuel
https://www.sciencedirect.com/science/article/microbial electrosynthesis
https://biooekonomie.de/foerderung/foerderbeispiele/neue-mikrobielle-biofabriken-erschliessen
https://www.researchgate.net/publication/321135607_Microalgae_for_Industrial_Purposes
https://en.wikipedia.org/wiki/Microbial_electrosynthesis
https://link.springer.com/article/microbial electrosynthesis
https://www.intechopen.com/books/Biofuels – Challenges and opportunities
https://www.systembiologie.de/de/aktuelles/wissenschaft/biosprit
https://www.deutschlandfunk.de/bio-solarzellen-mit-cyanobakterien-von-sonnenlicht-zu-100.html
https://www.wissenschaftsjahr.de/2020-21/aktuelles-aus-der-biooekonomie/aktuelle-meldungen/maerz-2020/cyanobakterien-als-oelquellen
https://en.wikipedia.org/wiki/Biohydrogen
https://biooekonomie.de/nachrichten/neues-aus-der-biooekonomie/erster-laufschuh-aus-recycelten-industrieabgasen

Dieses Werk ist lizenziert unter einer Creative Commons Namensnennung – Weitergabe unter gleichen Bedingungen 4.0 International Lizenz.