V 1_2.1
Zucker ist nicht gleich Zucker
Zurück zur Übersicht: Versuche (V) Kapitel 2 siehe: Haftungsausschluss
Material:
Wasserbad mit Reagenzglaseinsatz (Alternative: Tipp 1), 1 Reagenzglasständer, 5 Reagenzgläser, Reagenzglashalter, wasserunlöslicher Filzstift, Spatel, dest. Wasser, 2 Tropfpipetten, Messpipette (10 mL), Pipettierhilfe, Becherglas 300 mL (Abfall-Sammelgefäß), Schutzbrille, Einmalhandschuhe, Papierhandtücher
Chemikalien:
| Chemikalien: Fehling I, Fehling II, Glucose, Fructose, Lactose, Saccharose (=Haushaltszucker) ⇒ Schutzbrille aufsetzen ⇒ Einmalhandschuhe benutzen ⇒ nur die angegebenen Chemikalien-Mengen verwenden |
 |
 |
 |
 |
Vorarbeiten:
Das zur Hälfte mit Leitungswasser gefüllte Wasserbad wird auf ca. 70oC erwärmt.
Fünf Reagenzgläser werden von 1 – 5 beschriftet und in den Reagenzglasständer gestellt.
In jedes Reagenzglas werden mit der Tropfpipette zuerst 10 Tropfen Fehling I und dann (neue Tropfpipette!!) 10 Tropfen Fehling II gegeben.
Danach werden die Reagenzgläser einzeln wieder herausgenommen, vorsichtig hin- und hergeschwenkt (Tipp 2), bis eine klare Lösung entstanden ist und dann in den Reagenzglasständer zurückgestellt.
Mit einer Messpipette werden dann in jedes Reagenzglas 2 mL dest. Wasser gegeben.
Durchführung:
In das Rgl. 1 wird mit Hilfe des Spatels Glucose (ca. Menge einer Erbse) gegeben.
In die Rgl. 2 – 4 werden jeweils Fructose, Lactose, Saccharose in der zuvor genannten Menge gegeben.
Achtung: Der Spatel muss nach jedem Gebrauch mit Wasser abgespült und mit einem Papierhandtuch abgetrocknet werden!
In das Rgl. 5 wird nichts weiter hinzugegeben.
Durch erneutes Schwenken jedes Reagenzglases werden die darin enthaltenen Stoffe vermischt.
Die Farbe jeder Probe wird notiert.
Es macht nichts, wenn die Zucker noch nicht vollständig gelöst sind.
Die Reagenzgläser werden in das vorbereitete Wasserbad gestellt.
Nach ca. 4 Minuten werden die Reagenzgläser nacheinander mit dem Reagenzglashalter entnommen, nochmals leicht geschwenkt und wieder in den Reagenzglasständer zurückgestellt.
Die Farbe jeder Probe wird erneut notiert.
Beobachtung:
| Rgl Nr. | Inhalt FI/FII und … |
Farbe (vorher) |
Farbe |
| 1 | Glucoselösung | ||
| 2 | Fructoselösung | ||
| 3 | Lactoselösung | ||
| 4 | Saccharoselösung | ||
| 5 | 2 mL dest. Wasser |
Formuliere anschließend ein Ergebnis.
Die Inhalte der Reagenzgläser werden in das Sammelgefäß gegeben.
Ergebnis:
Hilfe für die Ergebnisformulierung:
Die sogenannte Fehlingprobe ist eine Nachweismethode für bestimmte Zucker.
Bei Vorhandensein dieser Zucker verändert sich die blaue Farbe des Gemisches in eine grünliche bzw. dann rötliche/rote Farbe.
Anhand der jeweils beobachteten Farbe kann beurteilt werden, ob ein Zuckernachweis erfolgt ist.
Das Ergebnis wird in der folgenden Tabelle notiert. Folgende Symbole sind zuzuordnen:
+ = Zuckernachweis / – = kein Zuckernachweis
| Rgl.Nr. | 1 | 2 | 3 | 4 | 5 |
| + / – |
Fehlerdiskussion:
Entsorgung:
Da es sich bei Fehling I um eine verdünnte Kupfer(II)-Sulfat-Lösung handelt, müssen die Inhalte der Reagenzgläser im Schwermetallabfall entsorgt werden.
Hilfen zu 3. (verkürzt/vereinfacht):
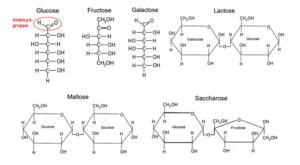
a- Die folgenden Abbildungen zeigen die Strukturformel (Kettenform / Ringform) der verwendeten Zucker.
b- Die Fehlingprobe ist ein Nachweis für das Vorhandensein einer Aldehydgruppe. Diese Gruppe ist verantwortlich für die Verfärbung von blau zu grünlich bzw. rötlich/rot. Sie reagiert mit dem Kupferanteil im Fehlinggemisch. Zucker, die zu dieser Reaktion führen, werden als „reduzierende Zucker“ bezeichnet.
c- Das Monosaccharid Fructose kann sich in Lösung durch Umgruppierung der Atome in Glucose umwandeln.
d- In Lösung kommen sowohl die Kettenform als auch die Ringform der Monosaccharide vor.
e- Bei Disacchariden können in Lösung die monosacchariden Bestandteile offenkettig vorkommen.
| Genauere Informationen zu den zugrundeliegenden chemischen Sachverhalten findest du hier: http://www.chids.de/versuche/protokolle/fructose_saccharose_glucose.pdf http://de.wikipedia.org/wiki/Reduzierende_Zucker http://de.wikipedia.org/wiki/Fehling-Probe |
Lösungen:
|
Tipp 1:
Falls kein Wasserbad zur Verfügung steht: regulierbare Heizplatte, Becherglas (200 – 300 mL) benutzen.
Achtung: Die Reagenzgläser schwimmen auf, deshalb einen Reagenzglashalter an jedem Reagenzglas befestigen und dann hineinstellen!
Darauf achten, dass das Wasser heiß ist, aber nicht kocht.! Gegebenenfalls mit einem Thermometer prüfen!
Die Erwärmung der Proben sollte nicht über der Bunsenbrennerflamme erfolgen!
Bei zu wenig Erfahrung mit dieser Methode besteht die Gefahr des „Herausschießens“ der Inhalte bei zu starker Erhitzung bzw. bei Siedeverzug.

Dieses Werk ist lizenziert unter einer Creative Commons Namensnennung – Weitergabe unter gleichen Bedingungen 4.0 International Lizenz.